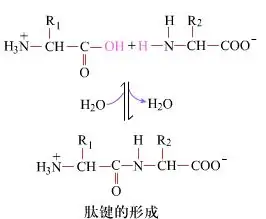
Nantu à a superficia, a furmazione di frutti di peptide, cedevanu di i tariffi di prucessu chimicu. Questu significa chì i dui cumenti aminuci acidi sò ligati da un bone peptide, un bone d'amide, mentre hè stata desidrata.
A furmazione di u bond di peptide hè l'attivazione di un amino acidu sottu e cundizioni di reazione leve. (A) Alietà di Carboxil, Seconda Amino Acino (b) u nucleofilicu attivatu mossietà carboxil attivatu dopu a forma di ueptide (A-B). "Se u cumpunente carboxyl (a) ùn hè micca prutettu, a furmazione di u Bond Peptide ùn pò micca esse cuntrullatu". Prodotti cum'è e peptidi lineali è ciclici ponu esse mischiati cù u target cumposti a-b. Dunque, tutti gruppi funziunali micca participati à a funzione di u bone Beettide in modu temporaneamente recente durante a manera di peptide.
Cusì, i sintesi di Pettiche - a furmazione di ogni peptide Bond - implica trè passi di aggregazione.
U primu passu hè di preparà certi amaggio chì hà bisognu di a prutezzione, è a struttura esse d'Amino Ididichi ùn si sò più esce.
U sicondu passu hè una reazione di dui petti per formà i ligami di peptide, in u quale u gruppu carboxil di u n-prutettu sò attivatu à l'intermediu attivu è poi u bond di peptide hè furmatu. Questa reazione accoppiata pò accade cum'è una reazione di un passu o cum'è duie reazzioni sequenziali.
U terzu passu hè a rimuzione selettiva o rimozione completa di a basa protettiva. Ancu se tutti i cacciatori ponu accade solu dopu tutti i piatti di POPPIDU, sò stati riuniti, eliminamentu di i gruppi di prutezzione hè ancu dumandatu per continuà a sintesi di peptide.
Perchè 10 aminochieri (por, thrr, asp, cru, cra, club, sec, cy) Gruppi di funziunali, chì necessanu a sozione selitativa, fà a sintesi di u selitativi più cumplicatu. E basa di prutezzione tempurale è semi-permanenti deve esse distinti per via di e diverse esigenze per a selezzione. I gruppi di prutezzione tempurale sò usati in u passu prossimu per riflette a prutezzione temporale di l'amino acidu o carburi funziunali carbox. I gruppi protettivi semi permettenti sò eliminati senza interferisce cù i bonds peptide dighjà furmatu o amino frasi laterali, à volte durante a sintesi.
"Idealment, attivazione di a cumpunente carboxyl è una furmazione successiva di riazzioni di peptide) deve esse rapid. Formazione razziale, è i reattivi di molar è à l'allevuli". Sfurtunatamente, nimu di i metudi chimichi di appiccicanti suddisfà questi esigenze, è pochi sò adattati per sintesi pratica.
Duranti Lotichi di Pepediani chì sò i gruppi funziunali implicati in diverse opazioni sò generalmente ligate à u centru manuale, è ci hè un potenziale risicu di rotazione.
U passu finale in u ciclu di sintesi di u PIPIDE hè a rimuzione di tutti i gruppi protettivi. Eliminazione selettiva di gruppi protettivi hè impurtante per a curtazione di a catena di a peptida in più di u requisitu per a rimozione completa di a prutezzione in sintesi di dipeptide. E strategie sintetiche anu da esse previsti currettamente. Sicondu a scelta strategica, n pò caccià selettivamente u gruppi di prutezzione di α-Amino o carboxil. U terminu "a strategia" si riferisce à a sequenza di reazzioni di condensazione di l'amino amino individuali. In generale, ci hè una differenza trà a sintesi di sintesi graduale è a condensazione di frammentu. Sintesi di pepetti (cunnisciuti ancu "sintesi convenzionali") si mette in suluzione. In a maiò parte di i casi, allarga graduale di a catena Pestiva pò esse sintetizatu solu per aduprà a catena pasticiterize in sintesi Granti. Per sintesi più longhi, i moléculi di destinazione deve esse segmentati in frammenti appropritati è determinate chì ponu minimizà u gradu di differenza. Dopu chì i frammenti individuali sò fidanzati gradualmente, u compostu di destinazione serà unitu. A strategia di Sintesi di Peptide include la selezzione di u megliu è u più approcratu Sintesi prutnificiti cumprese a selezzione di a scumessa prutica è u megliu metudu prutetti è u megliu metudu di fratturu cunjugazione.
Tempu post: 2025-07-02